我的博文
嗜铬细胞瘤和副神经节瘤临床病理学特征
【摘要】
嗜铬细胞瘤和肾上腺外副神经节瘤是比较少见的神经内分泌肿瘤,具有独特的组织学和免疫组化特征。对于这些肿瘤,一个实用且可重复的危险度分层系统仍在研究中。在这个迅速发展的分子医学时代,病理医生必须为自己提供一个副神经节瘤和嗜铬细胞瘤分类的框架,并提出一些建议指导临床医生如何预测预后。
【概述】
嗜铬细胞瘤和副神经节瘤(PPGLs)是不常见的神经嵴起源肿瘤,估计每年发病率为0.4~9.5/100万,约有不到0.1%的高血压患者发生此病。根据不同的发生部位,它们的生物学和临床行为从良性到潜在的侵袭性都有很高的转移风险。目前的评分系统在评估转移风险和总生存率方面有不同的应用,这有助于病人护理和治疗的分层管理。尽管这些肿瘤大多是孤立性发生的,但它们显然与一些潜在的家族/遗传疾病有关。确定潜在遗传性癌症综合征的存在至关重要。对于确诊为PPGL的患者,基因检测和转诊至专科医院是必要的。更新的2017年世界卫生组织内分泌器官肿瘤分类将新定义、最新科学进展和新的基因发现写进了PPGL中。嗜铬细胞瘤这个术语现在被保留用于肾上腺内肿瘤,而肾上腺髓质外的类似肿瘤被定义为肾上腺外副神经节瘤,并根据其解剖来源进一步命名。此外,对于交感神经副神经节瘤,已经确立了的三个10%(10%为家族/遗传性,10%为恶性,10%位于肾上腺外)不再适用。最近报道的家族性嗜铬细胞瘤/副神经节瘤综合征的胚系突变使遗传性病变的百分比增加到30%以上。
【解剖分布与形态学】
嗜铬细胞瘤和肾上腺外副神经节瘤是神经嵴起源的内分泌细胞或器官发生的肿瘤,这些内分泌细胞或器官称为副神经节,它们位于人体多个解剖位置,根据位置和神经联系分为交感神经和副交感神经。它们沿副交感神经系统的膈下分支呈不对称和轴向分布,包括头颈和主动脉肺动脉区,并与交感神经肾上腺神经内分泌系统相互连接(表1)。副交感副神经节的最大集合处是头颈部的颈动脉体。这些小卵圆形结构位于颈动脉分叉的内侧,在正常状态下,它们的重量约为12毫克。另一些副神经节是微小的,重量不一。无论解剖部位,所有的副神经节组织形态几乎相同。它们的主要功能单位是嗜铬细胞或主细胞,这些细胞被分隔成小叶或巢状,也被称为细胞球(zellballen)。支持细胞有助于维持小叶结构,周围则是由周细胞、内皮细胞和雪旺细胞组成的毛细血管网。嗜铬/主细胞属于弥漫性神经内分泌系统,散在全身的神经内分泌细胞离散聚集,含有分泌颗粒和参与儿茶酚胺合成的酶。
表1:副神经节的解剖分布

【诊断】
临床表现:PPGL的临床表现多种多样。大多数嗜铬细胞瘤都能分泌和释放儿茶酚胺,而儿茶酚胺的分泌和释放又与这些肿瘤的临床症状和体征有关。95%以上的功能性嗜铬细胞瘤患者有持续性或阵发性高血压的不同症状,而其余患者血压正常。约有25%的患者出现典型的临床三联征(头痛、心动过速和出汗),不到一半的患者仅出现其中一种症状。其他非特异性的发现包括体位性低血压、苍白、震颤、便秘和心理症状,包括急性焦虑和惊恐发作。功能性嗜铬细胞瘤也可能通过肿瘤细胞分泌生物活性物质而引起内分泌副肿瘤综合征(PNSs)。最常见的PNS是由促肾上腺皮质激素或促肾上腺皮质激素释放激素驱动的库欣综合征。血管活性肠肽产生引起水样腹泻、低钾血症和胃酸缺乏综合征(achlorhydria syndrome),以及促红细胞生成素(EPO)分泌过多或EPO受体敏感性过高引起的红细胞增多症。与嗜铬细胞瘤不同,许多肾上腺外副神经节瘤无临床症状。虽然交感副神经节瘤通常是功能性的(因此可能是症状性的),但只有不到4%的头颈部副神经节瘤出现与儿茶酚胺分泌过量有关症状。因此,许多副交感神经副神经节瘤是通过影像学偶然发现的,或表现为生长缓慢的无痛性肿块。
生化检测:血清学检测甲氧基肾上腺素,尿液检测去甲肾上腺素、肾上腺素和3-甲氧基肾上腺素对嗜铬细胞瘤的诊断有一定的提示意义。实验室结果阳性患者需要适当的临床随访。
大体和镜下特征:肿瘤境界清楚但无包膜。切面实性,灰白色、粉红色到深棕红色,可有出血坏死和囊性变等。PPGLs大小不一,但平均范围在3~6厘米之间,这取决于解剖部位。少数嗜铬细胞瘤的最大直径超过10厘米。

图1 嗜铬细胞瘤:(A)大体切除标本显示一个境界清楚的棕褐色肾上腺髓质肿块。
显微镜下,PPGLs表现出轻微的组织学异质性。大多数具有典型的细胞球(zellballen)模式,由均匀的多边形嗜铬/主细胞巢形成,周围有支持细胞和形成良好的血管网。瘤细胞可呈腺泡状或器官样、巢状、梁状、束状或实性片状分布。当这些病变呈现非经典形态时,PPGL的诊断对于更广泛的鉴别诊断可能具有挑战性,特别是在体检小的部位,如中耳,标本通常显示挤压状。虽然不常见,但也可观察到其他结构形态,如小梁、弥漫性和血管丰富型。细胞学上,嗜铬/主细胞从具有颗粒状嗜伊红、嗜碱性胞质的单一的多边形细胞到嗜双色胞质和圆形泡状核的细胞,或具有明显的多形性、核内假包涵体或明显核仁的细胞。胞质内嗜伊红玻璃样小体常见。比较少见的情况是,可以观察到梭形细胞和嗜酸性细胞,但通常只占肿瘤的一小部分。坏死和核分裂象比较少见,如有则可能提示具有恶性行为。在任何情况下,出现非典型核分裂象都应该特别关注。恶性嗜铬细胞瘤的诊断标准是出现远处转移。在所有嗜铬细胞瘤中,9%以上为复合型。复合型嗜铬细胞瘤部分由神经源性肿瘤组成,如节细胞神经瘤(70%~80%)、节细胞神经母细胞瘤(10%~20%),少数为神经母细胞瘤或恶性周围神经鞘瘤。这些肿瘤可以散发性出现或作为综合征的一部分。大约17%的复合型嗜铬细胞瘤被诊断为神经纤维瘤病1型(NF1),其中一半以上表现为双侧肿块。

图2 嗜铬细胞瘤:(B)显示均匀一致的嗜铬细胞巢的特征性细胞球形态
免疫表型:嗜铬/主细胞表达神经内分泌标记物,如syn、CgA和CD56,但不表达上皮标记物。其他标记物,如儿茶酚胺(catecholamines)、NSE和NF也可以表达。若细胞不表达CgA,则应重新考虑PPGL的诊断。此外,当遇到PPGL的结构变异时,S100蛋白可以有助于识别支持细胞。SDH基因胚系突变时免疫组化可显示SDHB蛋白阴性表达。
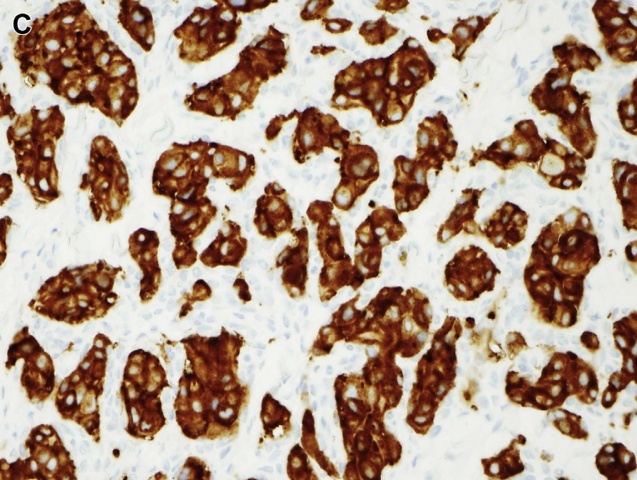
图3 嗜铬细胞瘤:(C)免疫组化显示嗜铬细胞强表达syn
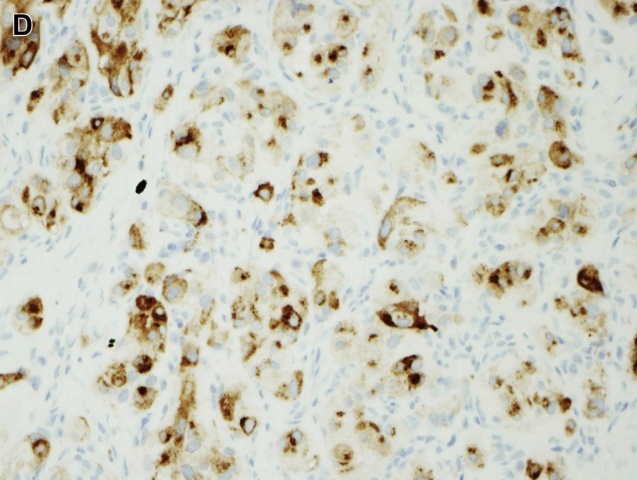
图4 嗜铬细胞瘤:(C)免疫组化显示嗜铬细胞表达CgA

图5 嗜铬细胞瘤:(C)免疫组化显示嗜铬细胞表达CD56
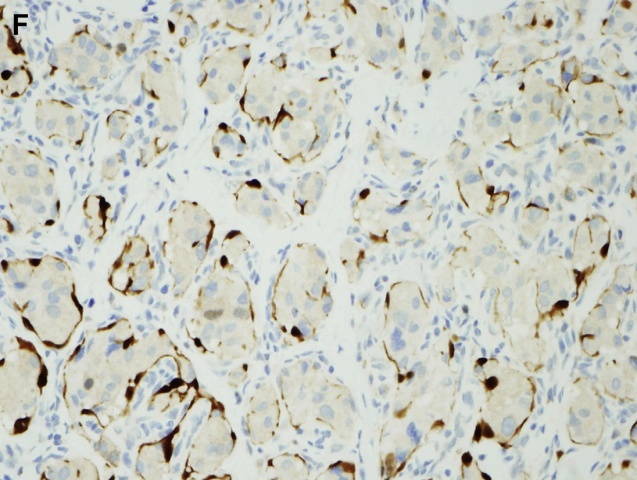
图6 嗜铬细胞瘤:(C)免疫组化显示支持细胞表达S100
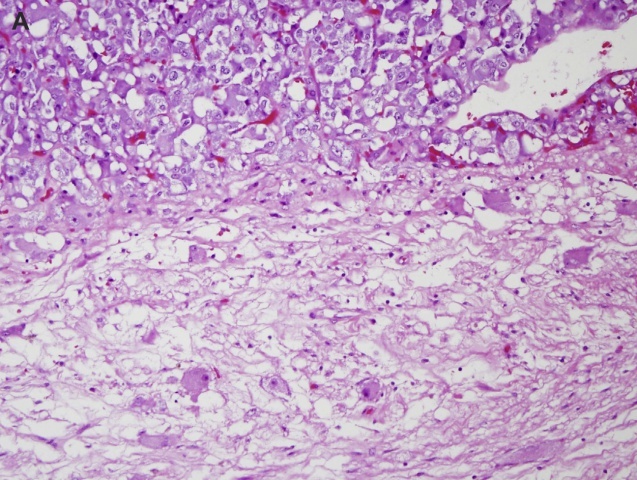
图7 复合型嗜铬细胞瘤:上部为典型嗜铬细胞瘤,下部见节细胞神经瘤中的大神经节细胞

图8 复合型嗜铬细胞瘤:上部为典型嗜铬细胞瘤,下部见节细胞神经瘤中的大神经节细胞
【生物学行为判定及风险评估】
新修订的世界卫生组织分类不再将嗜铬细胞瘤和副神经节瘤(PPGLs)分为良性和恶性肿瘤,都应被认为具有一定的恶性潜能(定义为具有转移风险)。在转移前确定某个PPGLs患者的风险程度更具挑战性。目前,还没有一个公认的共识能够确切预测这些肿瘤的恶性潜能。其中应用最广泛的分级系统是肾上腺嗜铬细胞瘤分级评分(PASS),仅适用于嗜铬细胞瘤;肾上腺嗜铬细胞瘤和副神经节瘤分级系统(GAPP),顾名思义,同时适用于嗜铬细胞瘤和副神经节瘤。
2002年,开发了PASS系统来识别有转移风险的嗜铬细胞瘤。通过评估12个最常见的转移性嗜铬细胞瘤的组织病理学参数和总和最大得分20分。大于或等于4分的肿瘤被定义为具有转移潜能风险;小于4分的为惰性肿瘤。8个组织学特征(大于肿瘤体积10%的弥漫生长的大巢、中心或融合性肿瘤坏死、细胞密度增加、纺锤形细胞、单一的生长模式、核分裂象增多(>3个/HPF)、非典型核分裂象和侵犯肾上腺周围软组织)各为2分。其余4个组织学特征(血管侵犯、包膜侵犯、巨大多形性核、核深染)各为1分。尽管PASS系统在预测转移潜能方面的实用性是有争议的,而且大多数内分泌病理医生对它的实用性不予重视,但它仍然得到了临床同事的认可,因此本文叙述一下而不推荐使用(本文作者不使用)。
最近证实,GAPP用于嗜铬细胞瘤和副神经节瘤,并结合了临床和组织学参数(表2)。GAPP提供了转移风险和患者生存率的逐步评估(stepwise assessment)。组织学分级是基于一个由6个考虑转移危险因素的参数组成的评分系统。这些参数是组织学模式、细胞丰富度(cellularity)、粉刺型坏死(comedo-type necrosis)、包膜或血管侵犯、Ki-67增殖指数和儿茶酚胺表型(catecholamine phenotype)。总分在0~2分之间的肿瘤被认为是高分化肿瘤。3~6分之间的肿瘤被定义为中分化。大于或等于7的分数被认为是低分化。大约70%的肿瘤GAPP评估是分化良好的PPGL,很少转移。中分化PPGL占PPGLs的20%,其余10%为低分化。中分化和低分化PPGLs与转移潜能增加有关,估计分别接近60%和88%。高分化、中分化和低分化PPGLs患者5年生存率分别为100%、67%和22%。与PASS相似,由于某些参数是主观的,GAPP的重复性是不确定的,因此它并没有被广泛用作预测工具。然而,由于验证研究是最近报道的,因此治疗PPGL患者的医生可能会要求使用GAPP这个系统这种评估。

图3 PPGL的风险评估:(A)嗜铬细胞瘤浸润肾上腺周围脂肪组织

图4 PPGL的风险评估:(B)血管侵犯也是转移风险增加的一个特征
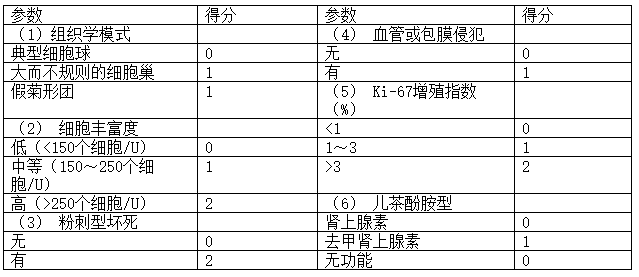
表2:肾上腺嗜铬细胞瘤和副神经节瘤分级系统(GAPP)
缩写:U,在高倍镜下(×400)观察单位面积10平方毫米的肿瘤细胞数。
【分子生物研究进展】
虽然大多数PPGLs是散发性病例,但已知易感基因的胚系突变在高达24%或散发性PPGL病例中发现。至少发现有19个遗传易感基因,即NF1、ATRX染色质重塑基因(ATRX Chromatin Remodeler,ATRX)、HRas原癌基因、GTPase(HRA)、VonHippel-Lindau(VHL)、内皮PAS结构域包含蛋白(EPAS1)或HIF2α、细胞周期蛋白依赖性激酶抑制剂2A(CDKN2A)、在转染期间重新排列(rearranged during transfection,RET)、肿瘤蛋白p53(TP53),肝细胞生长因子前体(MET)、丝氨酸/苏氨酸蛋白激酶B-Raf(BRAF)、myc相关的X因子(MAX)、异柠檬酸脱氢酶1(isocitrate dehydrogenase 1,IDH1)、类运动蛋白KIF1B(kinesin-like protein KIF1B)和琥珀酸脱氢酶(SDH)亚单位。
【遗传性癌症综合征】
以前认为嗜铬细胞瘤有10%与家族综合征有关;然而,目前已知高达24%的散发性PPGLs存在胚系突变。家族性PPGLs通常是多灶性或双侧性,发生年龄通常比在散发性PPGLs更早(常在20岁之前),后者通常发生在40岁之后。遗传性PPGLs常与其他肿瘤发生有关,一些遗传性疾病与PPGL的发生有关(表3),其中最常见的是多发性内分泌肿瘤2型(MEN2)、von Hippel-Lindau(VHL)、NF1和家族性嗜铬细胞瘤/副神经节瘤综合征(FPPGL)。

表3:嗜铬细胞瘤和副神经节瘤的遗传综合征

图4 具有VHL综合征患者的PPGL:瘤细胞透亮,细胞核轻度异型
我要评论




共0条评论