我的博文
组织细胞起源疾病(5)——肿瘤性病变(LCS)
作者:刘芳
这一讲我们主要专注于恶性Langerhans细胞疾病和Langerhans 细胞肉瘤。Langerhans 细胞肉瘤(LCS)是一种高级别肿瘤,具有真正恶性细胞学特征和Langerhans细胞表型。
具有Langerhans细胞特征表型的细胞可出现3种形态LCS:
一、LCH转变为肉瘤
极少数病例属于这种类型,几乎均为成年人,初次发作时具有LCH的临床和组织学特点,随后反复发作,保留CD1a免疫表型。此时怪异或间变细胞增加,非典型核分裂像也增加。最终进展为明显异型的肉瘤,此时既可出现CD1a表达,也可缺失。
二、具有侵袭性临床行为的Langerhans细胞病变
继发于T细胞性ALL,通过T细胞受体γ基因重排,白血病和继发性LCH都可以出现Langerhans细胞单克隆性增生,部分病例还表达CD56,有助于识别具有侵袭性临床行为的LCH。
三、原发性LCS
几乎均为成人。50%患者表现为广泛的肿块、转移,预后差。细胞显示恶性特征,包括多形性、非典型核分裂像,仍具有Langerhans细胞的免疫表型,染色可能不如LCH的细胞均匀一致。
具有Langerhans细胞特征的皮肤和软组织肉瘤可发生于单核细胞白血病和骨髓增生异常综合征(MDS)患者。少见情况下,在成人表现为真皮深部或皮下结节。病变中出现组织细胞和CD1a阳性细胞,有时围绕中央坏死区排列。然而这并不是LCH,而是单核细胞白血病或MDS在皮肤的表现,皮肤病灶内Langerhans细胞一般是成熟的。
Langerhans 细胞肉瘤(LCS)
流行病学
尽管只是个别病例报道,此种疾病与LCH无明显相关性,而是一种全新的肿瘤。LCS很罕见,虽然有较年轻LCS患者被报道,但几乎所有报道的患者均为成年人。近期有学者复习了53例LCS,发现患者年龄在 7-88 岁之间 (平均年龄50岁)。男:女= 3 : 2。罕见病例与滤泡性淋巴瘤有关,也有报道一些病例出现BRAF V600E 突变。测序研究发现一部分病例存在默克尔细胞多瘤病毒。
临床特征
皮肤及皮下软组织是最常见侵犯的部位。多器官侵犯多影响淋巴结、肺、肝、脾、软组织和骨,出现单一病灶或者多发病灶的LCS的比例大致相同。许多病例都是结外病变(侵犯皮肤和骨)和多灶病灶。>40%的病例都是临床分期为III-IV期。仅20%的病例原发于淋巴结。22%的患者有肝脾肿大,11%存在全血细胞减少。
形态学
最明显的特征是,出现真正恶性的细胞学特征,包括细胞密度高,具有明显核多形性,有时仅靠免疫表型和/或超微结构能够看出是LC来源。染色质块状,核仁明显。仍可见Langerhans细胞复杂皱褶核及核沟,胞浆中等丰富,这仍然是一个很重要的诊断线索。少量嗜酸性粒细胞散在分布。核分裂像可以较高, > 50个/10 HPF, 而且CD207阳性细胞中 Ki67>30%。当淋巴结被累及时仍是窦内侵犯。
免疫表型
从定义来看, Langerhans 细胞表达CD1a, CD207和S100。与LCH相比,LCS 的瘤细胞表达Langerhans细胞抗原的数量更是差异很大。而且随着疾病的复发,这些抗原会出现进行性丢失。 CD30 很少阳性,而CD56阳性预示预后不良,但并不是有效的运用。具有LCS特征的肿瘤可以在急性淋巴细胞性白血病或滤泡性淋巴瘤之后发生,其与这些淋巴瘤具有相似的分子遗传学特征。Langerhans细胞特点也可发生在单核细胞白血病或骨髓增生异常综合征的患者髓外肿瘤中,似乎具有异常分化。这不同于LCH治疗后发生的明确诊断的白血病。
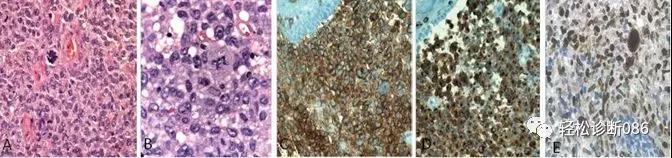
图1 Langerhans 细胞肉瘤。 A, 瘤细胞比LCH更密集,可见到核分裂像,包括罕见的不典型类型。B,细胞簇比LCH更多形性,亦见不典型核分裂像,提示高级别肿瘤。C, 瘤细胞表达CD1a. D, 瘤细胞表达 CD207 (langerin)。E. Ki67增殖指数比较高。
起源与预后
Langerhans 细胞肉瘤起源于一种成熟的Langerhans 细胞,具有BRAF V600E 突变。LCS 是一个侵袭性高级别肿瘤,一般以上患者死于进展期疾病。
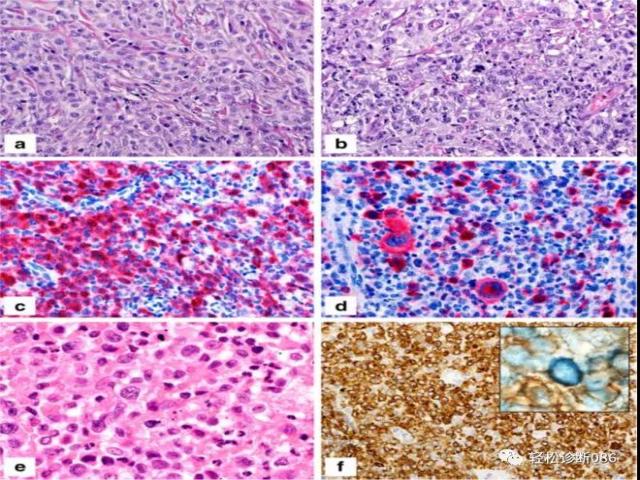
图2.LCH和LCS. 图a 和图b 来自于同一病例的皮肤活检,分别显示 LCH和LCS的细胞形态学特征。图c和图d为CD207染色,显示相应的区域为阳性。该LCS病例曾有T淋巴母细胞性淋巴瘤(T-ALL) (图e), CD207强表达 (图f) 。同一肿瘤细胞共同表达 CD1a (褐色) 和 CD34 (蓝色) (图f, inset) (这张图没有T-ALL的区域)。
【来源:轻松诊断086 微信公众号】

我要评论





共0条评论