我的博文
多发性骨髓瘤(MM)基因异常(FISH)检测
——预后评估、风险分层及个体化治疗工具
多发性骨髓瘤(multiple myeloma, MM)是一种最常见的恶性浆细胞病,占造血系统恶性肿瘤的10%,其特征是单克隆浆细胞恶性增生并分泌大量单克隆免疫球蛋白,引起骨痛、病理性骨折、造血异常、单克隆球蛋白血症及肾功能受损等一系列临床变化。据美国癌症协会最新Cancer Statistics 2013的数据显示MM的发病率和死亡率较前均有明显增加,估计美国2013年将新增病例22350例,预计有10710例患者死亡。MM的发生发展中伴随着多种特异的细胞遗传学层次上的相关基因数目或结构的改变。细胞遗传学改变在 MM 发病机制中发挥重要作用,MM 常涉及多种染色体异常,主要为数目异常,染色体核型异常分为超二倍体和非超二倍体两大类,其中超二倍体常见染色体改变是+3、+5、+7、+9、+11、+15、+19、+2l。非超二倍体主要累及-8、-13、-14、-17、-22 等。在 MM 染色体异常中结构改变较少见,主要有 1 号(1p、1q,部分缺失或 1q 三体)、13q-、14q (多为与 14q32 有关的几种互补易位)等。临床上,MM患者的生存期差异很大,从数月到10余年不等,中位生存期一般为2~3年,染色体异常在MM中有很高的发生率,并且多为复杂异常,误诊率高达60%,需提高其异常检出率,因此迫切需要新的治疗方法。NCCN多发性骨髓瘤临床实践指南推荐:2013 年第1版MM NCCN首次将细胞遗传学检测写入指南,最新版的指南中延续了染色体异常的检测。初始诊断中的骨髓检查应包括对骨髓穿刺所取细胞进行常规染色体核型分析和荧光原位杂交检测(FISH)。用于预后评估的FISH标记物应包括t(4;14)、t(11;14)、t(14;16),17p13缺失,13号染色体缺失及1号染色体扩增。

MayoClinic依据msMART(the Mayostratification for Myeloma and Risk-adaptedTherapy,msMART)原则对骨髓瘤患者进行危险分层,而针对分层结果选择不同治疗方式。
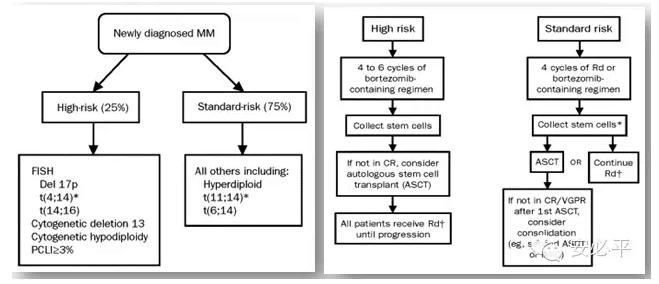
目前,国际上治疗一般先根据不同的临床及实验室指标评估病人的预后风险,然后为患者制定可靠地个体化方案。因而,明确MM分期及准确的预后风险评估指标至关重要。
FISH相关靶标介绍
荧光原位杂交(FISH)是行业公知的一项可用于染色体异常检测的方法,对于长片段的缺失、易位、拷贝数增加都有极佳的检测效果。
MM组合检测靶标包括:p53基因缺失、13q14缺失、1q21扩增和IGH重排。其中IGH重排和13q缺失是最常见的异常,其次为p53基因则认为是疾病进展中出现的继发性改变。
p53基因缺失 del(17p13)
探针名称: GSP p53
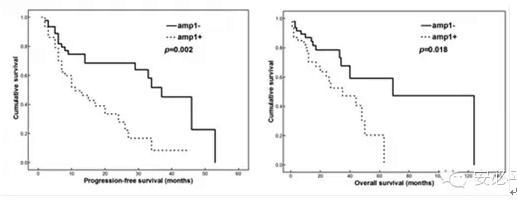
p53是肿瘤抑制基因,与细胞增殖调控、分化和凋亡相关,与肿瘤进展相关。p53基因缺失在MM中的发生比率9%~34%,有报道在中枢神经系统相关骨髓瘤中达到88.9%,阳性率可能与患者和靶细胞选择相关(例如anti-CD138抗体纯化浆细胞和形态学观察鉴别) [1,2]。p53基因与预后不良相关,缺失MM患者使用常规化疗方案预后差(图1,2),而进行高剂量化疗和自体干细胞移植(ASCT)后,仍表现不良预后,p53缺失较未缺失患者具更短的无进展生存期PFS (7.9个月 vs.25.7个月,P = .0324)和整体生存OS(14.7个月vs. 48.1个月,P = .0008) [3,4]。p53是MM独立预后指标。
13q14缺失 del(13q14)
探针名称:GSP D13S319和GSP RB1
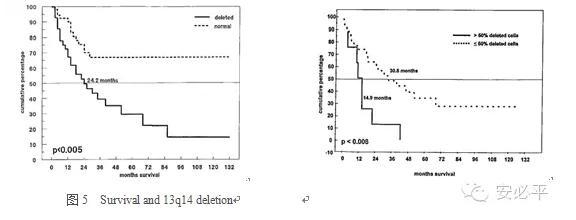
13号染色体长臂缺失(13q-)在MM患者中常发生,临床研究认为与较短的无事件生存期(EFS)和总生存期(OS)相关,染色体异常与未表现异常的患者EFS和OS有显著差异(p<0.001) [5]。13q14缺失对于常规化疗和反应差,生存更短(24.2个月vs. >60个月),高剂量化疗仍然预后不良,可作为对标准化疗方案不良预后的独立预后指标。
13q14缺失可能是MM发生中的关键事件,在相当大部分的stage I MM和未明的单克隆丙球病患者中发现13q14缺失,同时,13q14缺失细胞表现出明显的细胞增殖活性。FISH检测中常用于检测13q-的探针为RB1/D13S319(13q14)、distal deletions 探针D13S25 (13q14.3) 和D13S327(13q34)。13q缺失主要涉及13q大片段丢失或13单体,最常见缺失断裂点在 RB1 基因远端D13S272和D13S319区域。新发MM患者中RB1和D13S319缺失比率相近(46.2%和38.9%)[6]。 也有部分患者(13.8%)中出现13q34和13q14区域的同时缺失[7]和RB1/D13S319和D13S25共缺失(85%) [8]。
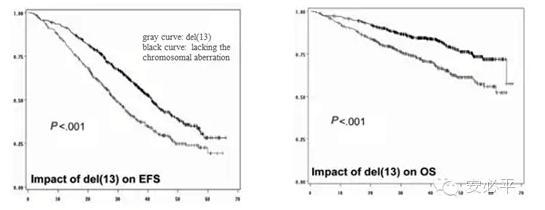
图3 Kaplan-Meier plot of the impact of del(13) on EFS for the 936 patients analyzed for this abnormality. | 图4 Kaplan-Meier plot of the impact of del(13) on OS for the 936 patients analyzed for this abnormality. |
1q21扩增 Amp(1q21)
探针名称:GSP 1q21
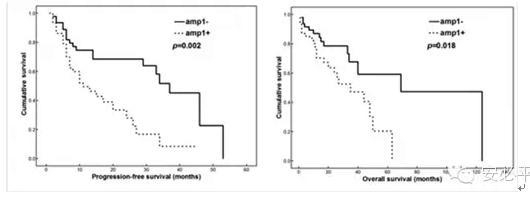
1号染色体异常常见于MM染色体异常中,其中主要为1q21区的串联重复和易位。临床研究发现1q21拷贝数增加/扩增伴随着MM的进展,与较差生存相关,随着疾病进展1q21增加的机率和拷贝数都会增加,是MM发病和进展中的关键遗传学事件[9],是硼替佐米(bortezomib)治疗后复发/难治性骨髓瘤PFS和OS的独立危险因素[10]。初诊MM患者中Amp(1q21)阳性率~40%,与预后差相关,未扩增患者反应率优于扩增阳性患者;其中部分会合并其它染色体异常,如del(13q14)、del(17p13) 和t(4;14)(p16;q32);当合并其它染色体异常时PFS和OS更短[11]。
IGH重排
探针名称:GSP IGH (双色断裂探针)
IGH基因(编码免疫蛋白重链)重排已经被证实是 MM 阶梯式分子发病学的早期事件,通常发生在 14q32 区域,断裂点主要在 D和 J 区,发生于约50%~60% MM 患者中。IGH 基因易位的伙伴染色体,主要包括 11q13(BCL1/CCND1)、4p16.3(FGFR3 )、16q23(MAF)、20q11(MAFB)和 6p21(CCND3)等,其中三个主要的为t(4;14)(p16.3;q32)、t(11;14)(q13;q32)和t(14;16)(q32;q23)。从临床角度看,最重要的是t(4;14)。一些研究证明伴有这种易位的患者预后差,平均生存期为24.7个月;t(11;14)易位或没有任何以上遗传学改变的患者接受常规化疗后平均生存期为50.5个月。
[与IGH重排相关的双色双融合检测探针]

FISH检测的意义
MM预后评估

[Fonseca R于2003年和2006年分别在 Blood和Leukemia发表有关遗传学亚组MM患者的生存期分析]
(1) 预后差: P53基因缺失、1q21基因扩增和IGH发生t(4;14) t(14;16)易位;
(2) 预后中等:13q14基因缺失;
(3) 预后好:IGH发生t(11;14)易位或者其他遗传改变。
MM风险分层及个体化治疗
美国Mayo Clinic提出了根据浆细胞指数,常规染色体核型分析及FISH检测骨髓瘤特异性的易位,将MM分为高危组,生存期短,治疗反应差,常表现为难治与耐药;标危组对药物反应较好。并提出相应的治疗策略:如建议初治高危、标危患者:初治高危患者采用硼替佐米为基础的治疗,标危患者则采用雷利度胺或沙利度胺联合其他药物治疗。
多发性骨髓瘤基因异常检测试剂盒(荧光原位杂交法)

British journal ofhaematology, 1999, 106(3): 717-719.
British journal of haematology, 2004, 127(3): 280-284.
Blood, 1998, 92(3):802-809.
Blood, 2005, 105(1):358-360.
Blood, 2007, 109(8):3489-3495.
Blood,2000,95(6):1925-1930,
Genes, Chromosomes and Cancer,2003, 36(1): 99-106.
Leukemia.2001,15(6):981-986.
Blood, 2006, 108(6):2020-2028
Bone Marrow Transplantation (2010) 45, 117–121.
Hematological oncology, 2013, 31(1): 41-48.
我要评论





共0条评论