我的博文
FISH在胶质瘤中的应用
胶质瘤是中枢神经系统最常见的原发脑肿瘤,也是目前神经肿瘤领域内的难点。传统的以形态学分类与分级不能准确反映胶质瘤的生物学特性。中国胶质瘤协作组经过一年多的酝酿,组织国内胶质瘤领域内的专家撰写了《中国脑胶质瘤分子诊疗指南》,并发表于《中华神经外科杂志》2014年第5期。指南的目的“建立以循证医学为基础的脑胶质瘤分子检测分析体系,描述最普遍的胶质瘤相关的分子改变、潜在的治疗靶点和生物标志物,从而用于指导临床实践并做出治疗选择。对于哪一个(类)患者或者样本需要进行检测,何时检测和如何检测,给出推荐”。
指南中涉及全面的分子靶标(IDH突变、1p/19q缺失、MGMT启动子甲基化、EGFR扩增、EGFRvⅢ重排、PTEN突变、TP53突变、BRAF融合、BRFA点突变、KI67、miR-181d等)检测,涵盖FISH、焦磷酸测序、PCR和IHC等多种分子检测技术(附表1)。
指南推荐FISH技术检测的靶标有:1p/19q缺失、EGFR扩增、EGFRvⅢ重排以及BRAF融合。FISH还可用于PTEN基因缺失的检测。
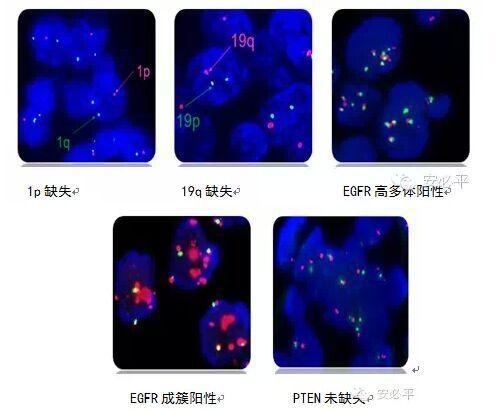
表1.11种胶质瘤分子标志物一览表[摘自指南]
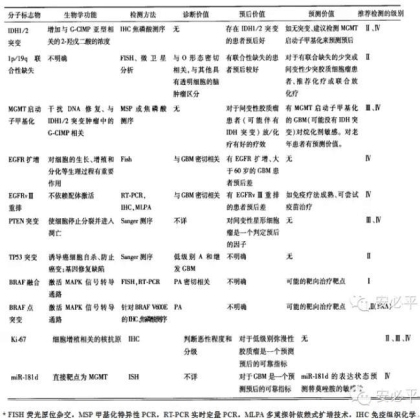
表2. 分子标志物对应胶质瘤病理类型
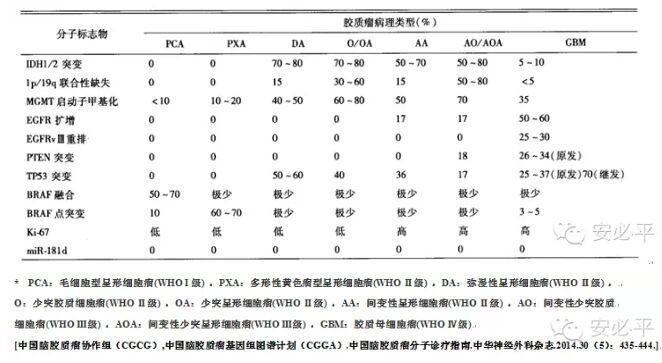
下面摘要与FISH相关的分子靶标进行简单说明:
一.1p/19q缺失
1p/19q联合性缺失在少突胶质细胞瘤中的发生率为80% -90%,在间变性少突胶质细胞瘤中发生率为50%-70% ,在弥漫性星形细胞瘤中发生率为15%,而在胶质母细胞瘤中发生率仅为5.0%。
lp/19q缺失检测可以辅助临床区分混合性少突星形细胞瘤更倾向于少突还是星形,这对于治疗选择有一定的意义。
存在lp/19q联合性缺失的少突胶质细胞瘤预后较好,肿瘤生长速度较慢,并对化疗敏感,特别是PVC化疗方案(丙卡巴肼,洛莫司汀,长春新碱)。
1p/19q缺失并伴有染色体多体相对于单纯的1p/19q缺失预后较差,复发可能性高。

二.EGFR扩增
间变性星形细胞瘤中EGFR扩增的发生率为17%,GBM中的发生率为50%- 60%,TCGA的经典型与Phillips增殖型和间质型的发生率高达94%。组织学上,小细胞GBM中GFAP表达很低,从形态学上难以和高级别的少突胶质细胞瘤相鉴别。
由于小细胞GBM中EGFR扩增很普遍,据此能鉴别诊断小细胞GBM与高级别的少突胶质细胞瘤。对于临床症状和神经影像学提示诊断为GBM的患者,由于取材的局限导致组织病例学上不能充分的证明是GBM,针对EGFR扩增进行检测就能确诊或排除GBM的诊断。
FISH可用于检测EGFR扩增,所以可作为判定肿瘤级别的一个备选指标。在临床上,60岁的CBM患者伴随EGFR扩增提示预后不良。
三.EGFRvⅢ重排
存在EGFR扩增的肿瘤可以伴发其他EGFR基因的改变,最常见的是外显子2-7框内缺失形成的EGFRvⅢ重排,EGFRvⅢ重排在GBM患者的发生率为20% - 30%。
EGFRvⅢ重排能够激活下游信号转导通路。EGFRvⅢ重排是否与预后相关还存在着争议,但是长期来看,有EGFRvⅢ重排的患者预后有差的趋势。
至今EGFR的靶向治疗对治疗GBM还没有明显的疗效,然而EGFRvⅢ重排给我们提供了一个靶向治疗的平台,多个二期临床试验已经发现针对于EGFRvⅢ重排的疫苗能够改善患者的预后。
四.BRAF融合
BRAF基因位于7q34,编码一种丝/苏氨酸特异性激酶,参与调控细胞内多种生物学事件,如细胞生长、分化和凋亡等。BRAF基因的串联重复导致了基因的融合,如KIAA1549-BRAF和FAM13IB-BRAF(少见)。
KIAA1549-BRAF融合在毛细胞型星形细胞瘤中高发(50% - 70%),而在其他级别胶质瘤或其他肿瘤中极为少见。KIAA1549-BRAF融合是一个重要的诊断标志物,由于毛细胞型细胞瘤也存在微血管的增生,在组织学上难以与CBM区分,如果检测有KIAA1549-BRAF融合则高度提示为毛细胞型星形细胞瘤。

五.PTEN缺失
PTEN基因定位于染色体10q23.3,PTEN是重要的抑癌基因。
PTEN参与了RTK/PI3K通路,86%的GBM患者会有包括PTEN基因缺失和突变的RTK/PI3K通路基因的改变。在原发性GBM中PTEN的点突变率为26% - 34%。间变性星形细胞瘤(18%)突变率明显少于GBM。有PTEN突变的间变性星形细胞瘤患者预后较差。
我要评论





共0条评论