我的博文
EGFR突变的耐药对策 
EGFR是一种跨膜受体,与细胞增殖、转移和凋亡等种信号传导通路有关。EGFR突变主要在外显子18-21,最常见的EGFR突变为外显子19缺失突变和外显子21点突变,均为EGFR-TKI的敏感性突变,外显子20的突变(除S768I和A763_Y764insFQEA之外)与EGFR-TKI耐药有关。EGFR基因突变的发生率在女性、非吸烟者、腺癌、亚裔人群中频率较高。肺腺癌患者EGFR基因敏感突变阳性率在亚裔人群和我国均为50%左右1,2,3。
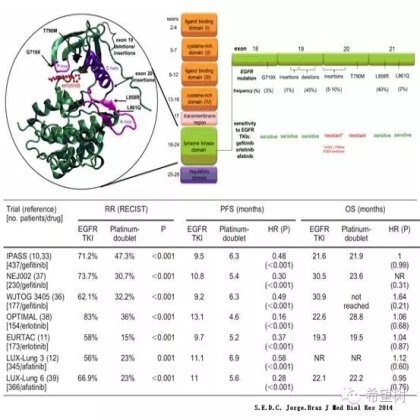
EGFR TKI 的疗效
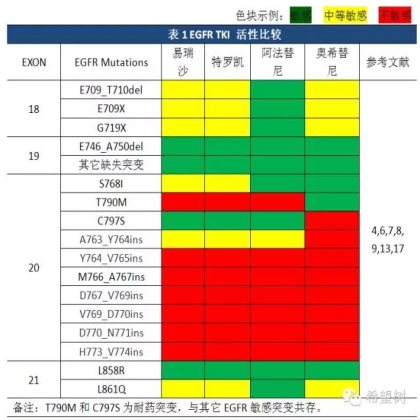
外显子19缺失突变和外显子21点突变(L858R)应用EGFR TKI疗效好于其它EGFR突变,外显子18突变其次4。而阿法替尼对外显子18突变等少见EGFR敏感突变的疗效强于其它EGFRTKI(易瑞沙、特罗凯和奥希替尼)5。
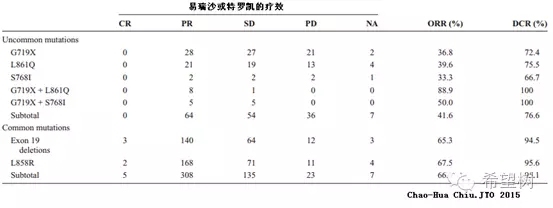
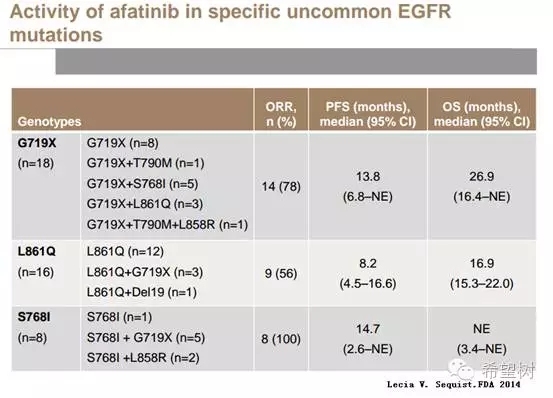
除A763_Y764insFQEA之外,外显子20插入突变应用易瑞沙、特罗凯、阿法替尼和奥希替尼无效,针对这一类型EGFR突变的Ariad公司研发的AP37288体外实验数据显示了良好敏感性,目前正在美国开展一期临床试验中(NCT02716116)6,7,8。
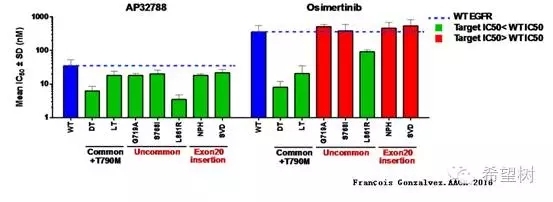
易瑞沙、特罗凯和阿法替尼耐药机制
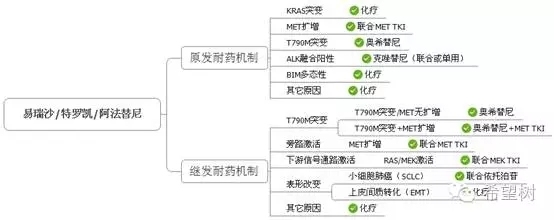
Camidge将EGFR TKI 耐药分为4 类,包括:①出现耐药突变,如T790M突变;②旁路激活,如MET扩增;③表型改变,如腺癌向小细胞肺癌转化,上皮细胞向间叶细胞转化(EMT);④下游信号通路激活,如BIM的多态性导致EGFR-TKI的原发耐药,通过MAPK1扩增直接激活下游增殖信号通路产生EGFR-TKI的获得性耐药2。
易瑞沙、特罗凯和阿法替尼50%的耐药机制是EGFR20外显子第790位点上的苏氨酸为蛋氨酸所取代(T790M),从而改变了ATP的亲和性,导致EGFR TKI不能有效阻断信号通路而产生耐药2,9。
Met扩增的耐药机制为Met与ErbB3结合,绕过EGFR激活下游信号通路,促使肿瘤细胞增殖,抑制凋亡。针对MET扩增的联合MET TKI多项临床试验取得了不错的疗效10。
其它突变基因共存也是原发耐药机制之一,比如KRAS基因突变和ALK融合阳性等2,11。
HER2扩增是否是EGFR TKI的耐药机制尚有争议。
奥希替尼耐药机制
奥希替尼是第三代口服、不可逆的选择性EGFR突变抑制剂。奥希替尼于2015年批准用于T790M突变非小细胞肺癌,患者用EGFRTKI治疗后进展患者的治疗,有效率59%12,13。
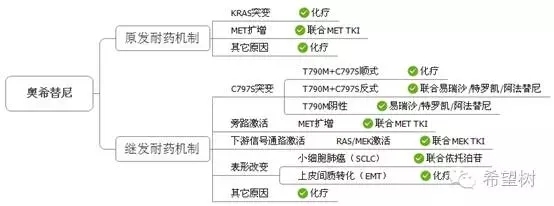
奥希替尼耐药机制包括:C797S突变,Met扩增,RAS/MEK下游信号通路激活,表现改变(转成小细胞肺癌或上皮间质转化)等14,15,16,17。
奥希替尼与半胱氨酸C797在ATP结合位点形成共价键,C797S突变影响了共价键的结合,类似BTK抑制剂依鲁替尼的耐药机制。一项针对15名奥希替尼耐药患者的研究发现,共有6名患者获得C797S突变(40%),均同时具有EGFR Del19+T790M。另一项针对67名奥希替尼耐药患者的研究发现,共有15名患者获得C797S突变(22%),均同时具有EGFR +T790M,C797S突变在EGFR 19突变的患者中比例比EGFR 21突变的患者中高的多(30%比8%)12。
C797S突变分三种情况,如果T790M和C797S两个突变在不同的染色体上,即反式模式,则可以使用易瑞沙、特罗凯或阿法替尼与奥希替尼联合使用方式。但如果T790M和C797S突变在同一个染色体上,也就是顺式模式,则对所有EGFR TKI耐药。还有一种情况是T790M阴性的情况下,直接出现了C797S,那么这个情况可直接使用易瑞沙、特罗凯或阿法替尼17。
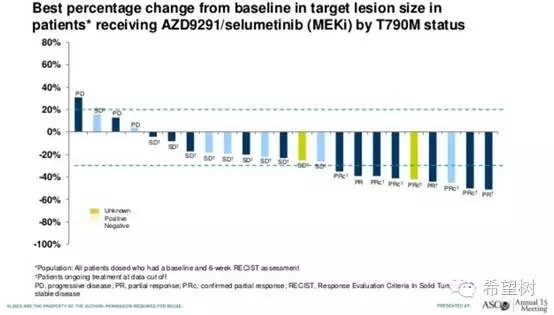
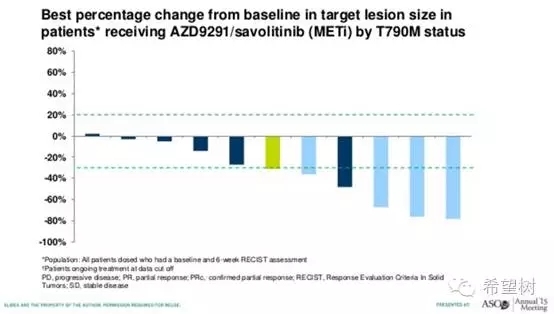
阿斯利康在2014年启动了TATTON(NCT02143466)一期多方案组临床试验,包括奥希替尼联合Selumetinib(AZD6244,MEK抑制剂),奥希替尼联合Savolitinib(MET抑制剂)16。
转自:https://mp.weixin.qq.com/s?__biz=MzIzODA5NDUzNw==&mid=2648633142&idx=1&sn=7cfc7d2023e26cc8737409c43a5873fa&chksm=f114de90c6635786b80a62f9c21add7c86a1f0d7a392526651b401e8a2810494e30dd2b09b07&mpshare=1&scene=1&srcid=0219Q46d955VVCkJKFyh7x97&pass_ticket=4dQ2O0ZdmGvFZ2wr1WU3GruiM8YoMcKx1MdkW7r6Minbo4yorF3NTeaj8mg57ZvV#rd
我要评论





共0条评论