我的博文
临床结局与临床终点
来源:医脉通
临床结局与临床终点是肿瘤相关临床试验中最常见的概念,一个outcome,一个endpoint,看起来意思差不多,但其中乾坤你真的清楚吗?小编今天为您抽丝剥茧,详细盘点outcome和endpoint的概念区别,一网打尽肿瘤临床研究中常见的所有endpoint,以后再看不懂JAMA、Lancet、NEJM、BMJ别怪医脉通啊。
临床结局vs临床终点
临床结局包括
►感觉(feels)是指患者的身体感觉(例如症状)或感知的心理状态,患者可能感觉到的疼痛、发热或感到严重的情绪低落(如同抑郁一样)等。
►功能(function)是指患者成功的执行一项任务方式和在必需的日常生活中发挥的作用,患者完成日常生活中的一项任务专门活动所表现出的特定的能力(如,如厕、穿衣等)。
►生存(survives)是指患者疾病最终结局如生存期、残疾、功能丧失和某些重要的临床事件(如,心梗、骨折)等生存状况水平和特点,指那些对患者影响最大、最直接、患者最关心、最想避免的临床事件。
临床终点
在一个特定时间段内已经发现症状或功能水平,或反映患者感觉、功能或生存状态的临床特点或变化的观测与评价指标。
终点(endpoint)是一种用于评价一个临床试验中不同治疗组间治疗效果统计学比较结果的一种评价方法,终点往往被解释为通过测量的评估;但实际完整的终点指标应该包括资料收集的全面描述,以及支持特定研究目的的分析比较方法。
临床结局主要是反映对疾病干预治疗产生的结果,而临床终点更强调在特定时限内的临床试验中,对临床结局的观测与评价。
因此,肿瘤药物临床试验一般都使用临床终点概念。而临床终点指标是指能够反映患者感觉、功能或生存的特性或变化的指标。
主要临床终点终极盘点
总生存期(OS)
定义为从随机化开始到因各种原因导致病人死亡之间的时间,且是按意向治疗人群(ITT)计算。对于死亡之前就已经失访的受试者,通常将最后一次随访时间计算为死亡时间。这个终点精确可测,并有死亡日期提供依据,因此在终点评估时不会出现偏倚。
抗肿瘤治疗的最终目标是延长患者的生命,因此OS一直被认为是临床试验中疗效评价的“金标准”,是目前评价抗肿瘤药物最可靠的临床试验终点。但研究实施和分析中存在一些困难,如大型试验随访期较长、随后的抗肿瘤治疗可能会混淆生存期的分析等。
无进展生存期(PFS)
PFS定义为从随机分组开始至出现肿瘤客观进展或死亡之间的时间。关于肿瘤进展的明确定义非常重要,应在方案中进行详细描述。
对于一部分癌症如某些乳腺癌、宫颈癌等,患者生存时间可以很长,选择OS作为研究肿瘤药物疗效指标会大大延长试验时间、增加实验难度和干扰因素,从而影响实验结果。而且癌症的进展过程常出现各种各样让患者苦恼、痛苦的症状,因此延迟疾病的进展过程对患者来说是很有意义的,也是临床治疗过程中重要的目标。
PFS反映了肿瘤的生长,可以在证实生存期获益之前进行评价,不会受到后续治疗的混淆。
生活质量(QoL)
临床研究中,可通过特定的调查问卷和量表等方式对患者日常生活能力进行评价,从而对抗肿瘤药物治疗效果进行评价。现在一些临床试验中使用患者报告结果(Patient Reported Outcomes,PROs)作为评价生活质量的方法之一。
客观缓解率(RR)
客观缓解率是指肿瘤体积缩小达到预先规定值并能维持最低时限要求的患者比例。缓解期通常是指从开始出现疗效直至证实出现肿瘤进展的这段时间。一般定义客观缓解率为完全缓解加上部分缓解之和。通常使用扫描或X射线测量肿瘤尺寸变化评价抗肿瘤治疗效果。若治疗后肿瘤缩小,则认为抗肿瘤治疗有效。
常用国际认可的RECIST v1.1(实体瘤疗效评价标准)指南评价缓解率:
►完全缓解(Complete response,CR):所有靶病灶消失,全部病理淋巴结(包括靶结节和非靶结节)短直径必须减少至<10 mm。
►部分缓解(Partial response,PR):靶病灶直径之和比基线水平减少至少30%。
►疾病进展(Progressive disease,PD):以整个实验研究过程中所有测量的靶病灶直径之和的最小值为参照,直径和相对增加至少20%(如果基线测量值最小就以基线值为参照);除此之外,必须满足直径和的绝对值增加至少5 mm(出现一个或多个新病灶也视为疾病进展)。
►疾病稳定(Stable disease,SD):靶病灶减小的程度没达到PR,增加的程度也没达到PD水平,介于两者之间,研究时可以直径之和的最小值作为参考。
►疾病控制率(Disease control rate,DCR)或临床获益率(clinical benefit rate,CBR):指经治疗后获得缓解(PR+CR)和病变稳定(SD)的病例数占可评价例数的百分比。
简而言之即DCR=CRR+PRR+SDR。疾病控制率与缓解率的区别在于:由于病变稳定(SD)也属于治疗有效的一种结果,故DCR将病变稳定的病例数记录在内,作为判断疗效的指标,较缓解率更为科学。
►缓解期(Duration of response,DR):从第一次出现完全缓解或部分缓解,到第一次诊断疾病进展或复发的时间。
其它终点
活动状态评分(Performance status,PS)
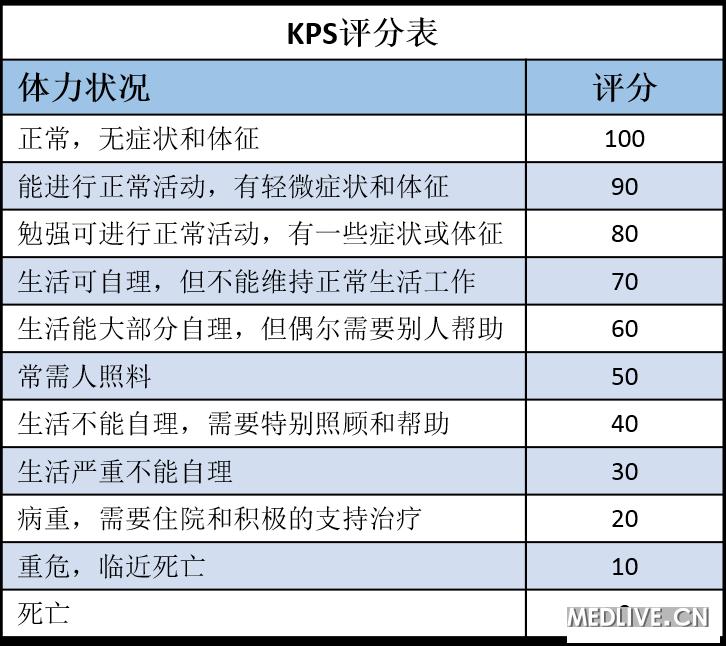
对癌症患者在接受治疗前、治疗期间和治疗后日常生活能力的评估。即从患者的体力来了解其一般健康状况和对治疗耐受能力的指标。常用美国东部肿瘤协作组评分表和卡氏评分表进行评估。
►美国东部肿瘤协作组评分表(The Eastern Cooperative OncologyGroup,ECOG),一般认为活动状况3、4级的病人不适宜进行化疗。
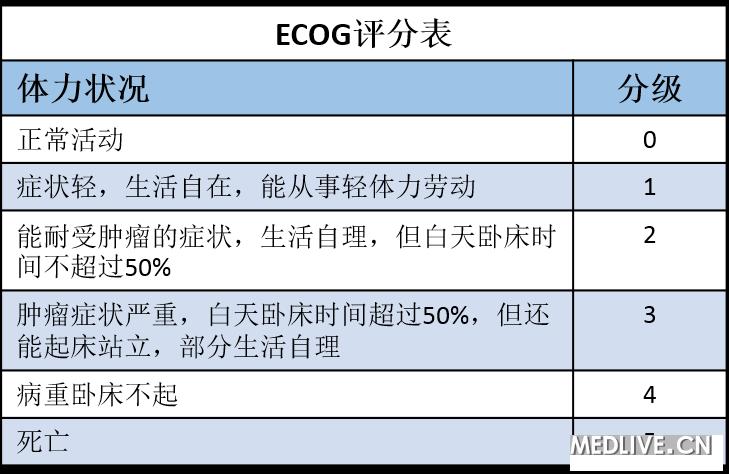
►卡氏评分表(Karnofsky status,KPS),评分若在40%以下,治疗反应常不佳,且往往难以耐受化疗反应。
至疾病进展时间(Time to progression,TTP):
TTP定义为从随机分组开始至出现肿瘤客观进展之间的时间,不包括死亡。在对TTP的分析中,无论是在死亡时还是相对较早的随访期间,死亡均被删失(试验中的非随机脱落)。当大多数死亡与癌症不相关的情况下,TTP也可以是一个合适的终点指标。
无病生存期(Disease/recurrence free survival,DFS):
通常定义为患者从随机分组开始到出现肿瘤复发或由任何原因引起死亡之间的时间。该终点最常用于根治性手术或放疗后的辅助治疗的研究。
当生存期延长而使得选择生存期为临床试验终点不现实的时候,DFS可以作为一个重要的终点指标。目前DFS已经成为乳腺癌辅助性激素治疗、结肠癌辅助治疗、以及乳腺癌的辅助性细胞毒治疗的主要审批基础。
无远处转移生存期(Distant disease/recurrence free survival,DDFS):
指肿瘤患者经过治疗后除了原发病灶意外,未发现全身其他地方有转移病灶的一段时间。
无侵袭性疾病生存期(Invasive disease free survival,IDFS):
侵袭性疾病患者在接受辅助治疗(对主要治疗方案的补充,如手术后化疗等,旨在清楚可能残存的癌细胞以延缓或防止疾病复发)后至疾病复发的时间。
微小残留病灶(Minimum residual disease,MRD):
指癌症患者在治疗中或治疗后仍有残留的恶性细胞存在,是癌症复发的主要原因,如白血病。
无事件生存(Event free survival,EFS):
指从入组开始到预定”事件“发生的时间,“事件”可包括死亡、疾病进展、改换化疗方案、改为化疗、加用其他治疗、发生致死性或不能耐受的副作用等种种事件。主要用于病程较长的恶性肿瘤、或该实验方案危险性高等情况下。
病理完全缓解(Pathologic complete response,pCR):
指癌症患者在治疗后病理检查未发现有癌细胞残留。
末尾干货,超清大图总结对比:(点击查看大图)
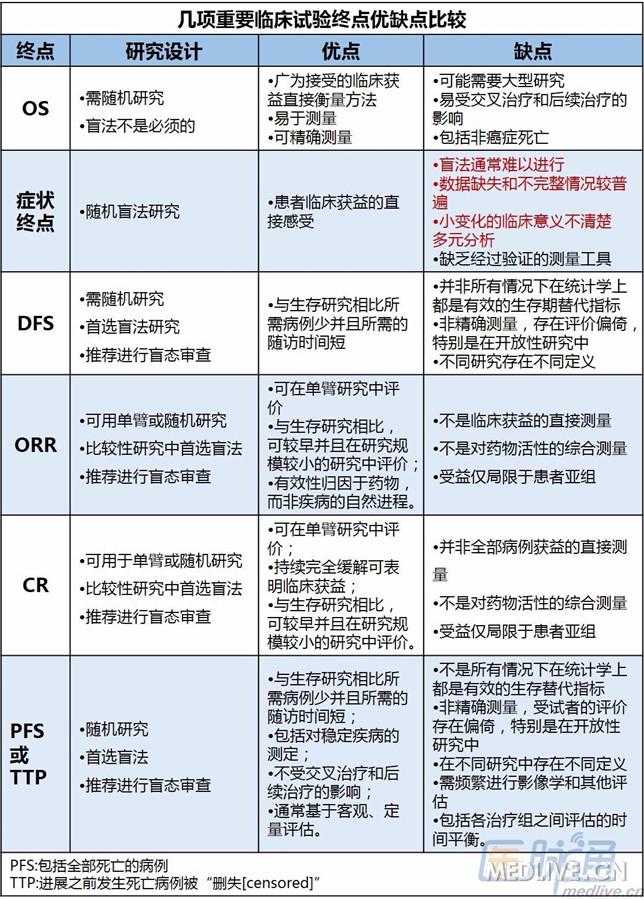
主要参考文献:
1.Understanding Clinical Trials.Roche.com
2.抗肿瘤药物临床试验终点技术指导原则. Sda.gov.cn
3.刘炳林. 药物临床试验中有效性指标的分类[J].中国新药杂志,2016,10:1103-1107.
我要评论





共0条评论