我的博文
【JCO】MET exon14缺失突变可能为肺肉瘤样癌的潜在作用靶点 
key point:
MET exon14突变有望成为肉瘤样癌的治疗靶点。
肉瘤样癌占肺癌0.1-0.4%,对化疗不敏感,预后较差。该研究采用全外显子测序,检测已知的驱动基因并探索可能的新靶点。
【方法】
1.研究设计
共筛选41例病理确诊肺肉瘤样癌患者,常规检测EGFR/ALK/KRAS/BRAF基因。36例患者标本符合基因检测要求,其中,10例具有足够肿瘤组织冰冻/包埋标本及正常组织冰冻标本患者进入探索集;余26例患者为验证集。研究流程图见图1.

图1研究流程图
【结果】
1. WES测序后分析挑选出15个重要的突变基因进行验证
采用TrueSeq平台或Sanger测序在10例探索集中检测这15个基因,其中9个基因为已知的癌基因或抑癌基因:TP53(6/10),PIK3CA(2/10),MET(2/10),KRAS(2/10),STK11(1/10),SMARCA4(1/10),RB1(1/10),NOTCH1(1/10),MLL2(1/10);6个为新发现的突变基因:RASA1(2/10),CDH4(2/10),CDH7(2/10),LAMB4(3/10),SCAF1(2/10),LMTK2(2/10)。
2. 靶点筛查发现MET基因突变频率较高
MET基因突变发生在exon14,其编码MET蛋白跨膜区。研究者MET基因exon14进行双向测序,在26例验证集患者中发现6例子患者MET exon14结合点体细胞突变。METexon14的突变率为22.2%(8/36)。图2示MET突变模式图(摘自原文)。
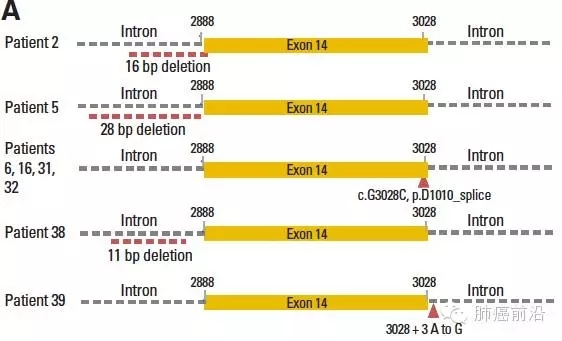
3. MET exon14突变使得转录后的mRNA无exon14,产生了蛋白异构体。
4. MET exon14突变患者的特征
MET exon突变与其他驱动基因如EGFR、KRAS、BRAF、ALK互斥,有1例患者合并有PIK3CA突变。8例MET突变患者,7例患者肿瘤组织中混合有腺泡样腺癌成分。
5. MET抑制剂作用于MET突变细胞株
Crizotinib能有效抑制METexon14突变细胞株Hs746T的生长,且下游Akt/MAPK蛋白表达下调;同时合并有MET exon14和PIK3CA突变的细胞株HCC827,Crizotinib抑制作用不明显。RNA干扰结果同crizotinib。同时应用crizotinib和PIK3CA抑制剂(GDC0941)能有效抑制HCC827生长。
6. 1例MET exon14突变患者服用crizotinib后疗效显著,如图3示患者服药前后影像学变化(摘自原文)。
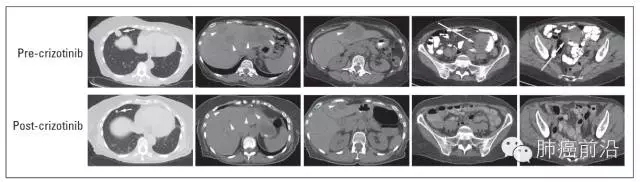
【结论】
MET基因突变导致exon14的转录后缺失在肺肉瘤样癌中常见,可能是肉瘤样癌有希望的治疗靶点。
【点评】
近两年来关于denovoMET异常已然成为研究的热点。MET活化形式多样,METamplification,MET overexpression,METmutation,究竟何在检测手段可作为界定MET活化的最佳biomarker,仍值得深思。该研究的设计思路可以为临床医生进行转化医学研究提高重要参考。MET exon14是否是真正的驱动基因,仍需要动物实验及临床更多病例研究的探索。自发现MET基因至今已有20余年,然而我们对MET基因的了解仍然非常局限,前期Metmab等研究的失败给很多研发者和临床肿瘤学家带来了沉重的打击。即便如歌词所言“多么痛的领悟”,我们对MET基因的研究仍然会坚持。
【文章来源及补充资料】
1. Liu X, Jia Y, Stoopler MB et al. Next-Generation Sequencing ofPulmonary Sarcomatoid Carcinoma Reveals High Frequency of Actionable MET GeneMutations. J Clin Oncol 2015.
2. TruSeq® Amplicon Cancer Panel利用212个扩增子来检测48个癌症相关基因中的突变区域,其中包括KRAS、EGFR及BRAF。TruSeq® Amplicon操作平台可检测频率低于5%的突变,一次可以同时运行96个样本的高度多重分析。
我要评论





共0条评论