我的博文
思考RAS状态在mCRC治疗中的意义
RAS突变状态对治疗选择的作用
表皮生长因子受体(EGFR)在一些肿瘤细胞中常过表达,而EGFR过表达状态与肿瘤细胞的转移、侵润、预后差等相关。EGFR下游的信号转导通路(图1)中主要的一条即为RAS/RAF/MEK/ERK-MAPK通路。除KRAS突变外,EGFR下游信号传导通路中多位点突变可能影响药物疗效。
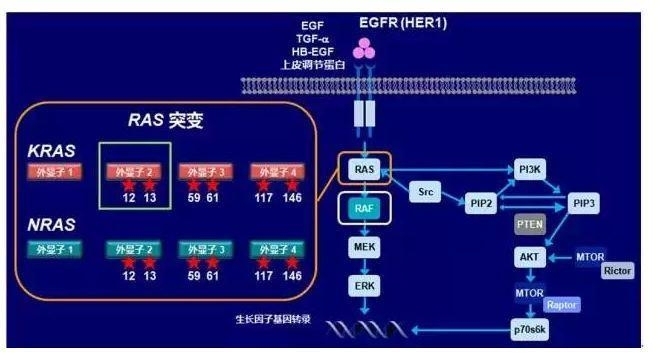
图 EGRF信号传导通路示意图
FIRE-3和CALGB80405研究是现已公布的针对靶向药物一线治疗KRAS野生型患者的头对头Ⅲ期研究,研究结果均证实,贝伐珠单抗和西妥昔单抗一线治疗晚期结直肠癌(mCRC)生存获益相似。
FIRE-3 Ⅲ期研究对比了西妥昔单抗与贝伐珠单抗分别联合FOLFIRI(伊立替康+5-氟尿嘧啶+亚叶酸钙)方案一线治疗mCRC患者的疗效,研究主要终点为总客观缓解率 (ORR)。
结果显示,在RAS野生型患者中,西妥昔单抗与贝伐珠单抗治疗的ORR获益相似(65.3%对58.7%,P=0.18)。次要研究终点无进展生存期(PFS)获益在西妥昔单抗与贝伐珠单抗的2组中也得到相似结果。但在两组患者结束一线治疗后总生存期(OS)的KM曲线开始分开,显示出统计学差异,中位OS分别为33.1个月对25.0个月[风险比(HR)为0.697,P=0.0059]。后续分析中显示,46.6%的西妥昔单抗组患者接受FOLFOX+贝伐珠单抗治疗,而41.4%的贝伐珠单抗组患者接受FOLFOX+西妥昔单抗治疗,该方案在mCRC治疗中被证实有效。因而,2组患者的OS差异或并非归功于一线治疗,后线治疗可能对整体OS产生影响。
另一项CALGB 80405研究同样比较了KRAS野生型患者接受贝伐珠单抗和西妥昔单抗这2种靶向药物联合FOLFOX(奥沙利铂+5-氟尿嘧啶+亚叶酸钙)方案/FOLFIRI方案的一线治疗疗效。
当前RAS突变检测还面临以下不足,亟需标准化。①检测位点不统一:对来自各随机临床试验的逾5000例患者进行荟萃分析显示,在KRAS野生型患者中仍有20%存在其他RAS突变,全RAS野生型患者比例下降。因此,全RAS检测需包括KRAS、NRAS等共6个外显子;②检测方法不统一:当前检测方法包括测序法、PCR法等,且不同方法灵敏度不同;③检测截点值尚未统一,采取不同截点值突变的比例将发生变化,从而使得RAS突变率产生差异。因此临床实践当中,在给予患者抗EGFR治疗之前,必须明确KRAS和NRAS状态,这也对我国很多医院的KRAS突变检测提出了更高、更新的要求。
我要评论





共0条评论