我的博文
前列腺原发性血管内大B细胞淋巴瘤病例报告及文献复习
【摘要】 目的 讨论原发于前列腺的血管内大B细胞淋巴瘤(intravascular large B-cell lymphoma,IVLBCL)的临床病理学特征、诊断及鉴别诊断、临床治疗及预后情况。方法 通过系统回顾分析我院1例原发于前列腺的IVLBCL患者的临床学资料、组织病理形态学和免疫组织化学分析结果,并进行相关文献资料的复习分析。结果 本例患者因排尿困难,查体时发现前列腺增生收入院,病理学检查发现前列腺间质小血管内可见成簇的异型淋巴样细胞,免疫组织化学示淋巴样细胞 CD20++、PAX5+、Ki-67增殖指数 70~75%,血管内皮CD34+。 病理学诊断是前列腺IVLBCL(非生发中心起源),患者5个月后死亡。 结论 原发于前列腺的IVLBC极为罕见,临床学表现缺乏特异性体征,容易造成漏诊或误诊,病理学检查及免疫组织化学对前列腺IVLBCL 的诊断和鉴别诊断具有重要的意义。
【关键词】 血管内大 B 细胞淋巴瘤;前列腺;诊断;免疫组织化学
IVLBCL在2016年最新版WHO淋巴样肿瘤分类学中被列为一种独立的疾病类型,属于罕见的高度侵袭性结外弥漫大B细胞淋巴瘤(diffuse large B cell lymphoma,DLBCL)的一个亚型。该肿瘤多好发生于中老年人,男女无明显差别,病变常多累及皮肤和中枢神经系统,也可侵犯肾、肺、肾上腺、胃肠道和脾脏等部位,但淋巴结、子宫、膀胱和前列腺等部位极少受累。其病理形态学特点为淋巴细胞样肿瘤细胞选择性生长在血管腔内,特别是毛细血管内,一般不会累及大中动脉及静脉。部分患者发病隐匿,生前未能做出正确的诊断,故多在其尸检过程中发现。我科室在临床外检工作中遇到1例发生于前列腺的IVLBCL,并结合国内外相关文献对其临床学表现、病理组织学特点及免疫组化结果进行讨论和总结,以提高临床对该肿瘤的认识。
1材料与方法
1.1材料 患者,男性,87 岁,因患者排尿费力,经门诊后收入我院泌尿外科。体检:体温36.6 ℃,血压 160/90 mmHg。未发现皮肤红斑及结节,无其他异常发现。 B超提示前列腺增生(大小3.9cm×4.5cm×4.1 cm,粗点状低回声,分布不均匀)。血常规检查显示红细胞总数 2.9×1012/L, 血红蛋白 85 g/L,白细胞计数3.29×109 /L,中性粒细胞 0.669×109 /L,淋巴细胞 0.195×109 /L;前列腺特异性抗原 0.077ng/ml,游离前列腺特异性抗原 0.020ng/ml;尿液检查:白细胞50.1/μl。 患者于入院后于截石位行经尿道前列腺激光电切术。
1.2方法 标本取材后经4%中性甲醛液固定,石蜡包埋,常规切片,HE染色,光镜下观察。免疫组化染色采用EnVision法,所用试剂采用北京中杉金桥生物技术有限公司。
2结果
2.1巨检 大体检查:送检(前列腺激光切除标本)灰白间灰褐色碎组织1堆,总大小6*5*2cm,质韧。
2.2镜检 光镜下:前列腺组织碎片内见扩张的毛细血管,血管内可见多量中-大淋巴样细胞,细胞异型性显著,细胞核呈卵圆形,染色质浓稠,可见少量胞浆,核分裂象可见,部分细胞退变、坏死(图1-3)。
2.3免疫组化 肿瘤细CD20和PAX-5弥漫(+)(图4和5),MUM-1、Kappa、CD5(图8)、Bc1-6和Bcl-2(+),CD31和CD34(血管+)(图9),Ki-67增殖指数+70~75%(图7),肿瘤细胞Cytokeratin、CD3(图6)、CD10、Lambda、CD38、CD56(-)。
病理诊断:前列腺原发性血管内大B细胞淋巴瘤,(非生发中心起源)。
该病人出院后转专科医院进一步接受化疗治疗,具体治疗方案不详,5个月后死亡。
3讨论
3.1临床表现
DLBCL是最常见的非霍奇金淋巴瘤(Non Hodgkins lymphoma,NHL),占所有NHL的30%~40%。IVLBCL属于一种高度侵袭性结外DLBCL,肿瘤细胞因只侵犯不同器官系统的小血管及毛细血管,使其临床症状变得多样复杂性和非特异性。其主要病理形态学表现为肿瘤细胞仅存在于人体系统器官的小血管内,特别是在毛细血管内,因侵犯器官的不同而出现出不同的临床症状。患者常可出现发热、乏力和体重减轻等症状,也可表现为受累器官的增生肥大,而实体性肿块实为罕见,也常无淋巴结肿大。大多数病例在临床初期的外周血及骨髓检查无明显异常发现,故此该肿瘤早期的诊断很困难,常发生误诊、漏诊和延迟治疗的情况。
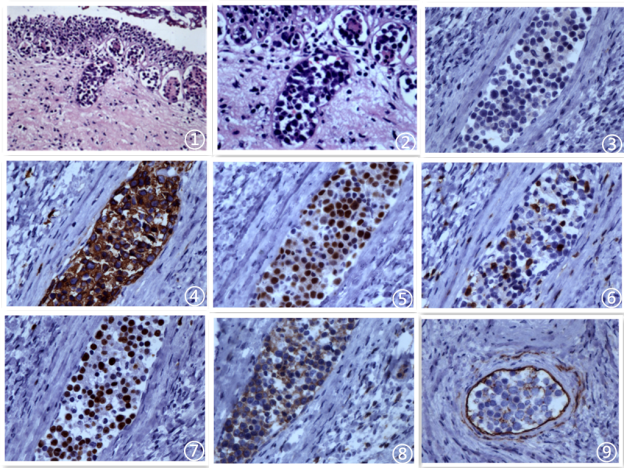
图1前列腺间质小静脉及毛细血管内可见成簇的异型淋巴样细胞 HE ×100;图2肿瘤细胞HE ×200;图3肿瘤细胞HE×400;图4肿瘤细胞CD20强阳性,EnVision法;图5肿瘤细胞PAX5阳性,EnVision法; 图6肿瘤细胞CD3阴性,背景散在阳性,EnVision法;图7肿瘤细胞Ki-67增值指数(+70~75%), EnVision法;图8肿瘤细胞CD5阳性,EnVision法;图9肿瘤细胞被CD34阳性的血管环绕,EnVision法。
表一 国内外前列腺血管内大B细胞淋巴瘤文献资料
作者 | 年龄 | 部位 | 症状 | 免疫组化结果 | 临床处理 | 预后 |
Chim C等2002 | 64岁 | 前列腺 | 前列腺增生 | CD45+, CD20+ | 未化疗 | 失访 |
Quintini G 2003 | 68岁 | 前列腺 | 前列腺增生 | CD45+, CD20+, CD79α+ | 未化疗 | 失访 |
Alfaro J等2004 | 78岁 | 前列腺 | 前列腺增生 | CD20+, CD79α+ | R | 24个月后症状缓解 |
尹秀荣等2005 | 66岁 | 前列腺 | 前列腺增生 | CD45+, CD20+ | 未化疗 | 2个月后死亡 |
Csomor J等2008 | 73岁 | 前列腺,淋巴结 | 前列腺增生,淋巴结肿大 | LCA+,CD20+ | R- CHOP | 30个月后死亡 |
杨春梅2008 | 78岁 | 前列腺 | 前列腺增生 | CD45+, CD20+ | 不详 | 不详 |
Pusch G等2009 | 64岁 | 前列腺、 脑 | 前列腺增生,中枢系统症状 | CD20+, MUM1+ | R- CHOP | 5个月后症状缓解 |
徐曼等2011 | 65岁 | 前列腺 | 前列腺增生 | LCA+, CD20+, CD79α+ | CHOP | 15个月后症状缓解 |
蒋萍等2017 | 84岁 | 前列腺 | 前列腺增生 | LCA+,CD20+, CD79α+ | 拒绝治疗 | 5个月后死亡 |
本例 2018 | 87岁 | 前列腺 | 前列腺增生 | CD20+、PAX5+ | 转院治疗,具体方案不详 | 5个月死亡 |
Pfleger和Tappeiner 等人曾于1959年首次报道该肿瘤,并将其命名为“皮肤系统性血管内皮瘤”,此后曾用名有“血管内淋巴瘤病、嗜血管性淋巴瘤”等。1986 年,Sheibani 等人通过免疫组织化学方法证实了其本质上是一种淋巴细胞来源的恶性肿瘤,因此曾称其为亲血管性(血管内)大细胞淋巴瘤 ( angiotrophic ( intravascular ) large cell lymphoma )。WHO于2001年正式将其作为一种肿瘤类型纳入并进行具体的描述 。2016年,最新版WHO血液和淋巴系统肿瘤分类将这一罕见类型的非霍奇金淋巴瘤,归类在成熟B细胞肿瘤分类中,属于一种弥漫大B细胞淋巴瘤的独特亚型 。
IVLBCL的年发生率约为(0.5-1.0)/1000 000,中位年龄62~70岁,男女之比为1.1:1。 临床主要分为两种类型 :(1)西方型:也被称为经典型,其临床表现与受累脏器有关,主要是侵犯中枢神经系统和皮肤;(2)亚洲型:也被称为嗜血细胞相关型,由日本学者 Murase 等人于1997 年提出,常见于东亚地区,其中以日本报道最多,其特点为多脏器系统衰竭、肝脾脏器肿大及嗜血综合征,而我国既往报道的 IVLBCL绝大多数倾向于西方经典型。该病病情进展非常迅速,对治疗反应差,临床预后多不良。文献报道在肾、肾上腺、膀胱、肺、肝、脾脏和子宫均可被累及,而发生于前列腺则极为罕见 。
前列腺是结外淋巴瘤发生的少见部位,其发病率<1%,前列腺IVLBCL则更罕见,目前国内外文献报道十余例。发病年龄64—87岁(平均73岁),无淋巴瘤的典型临床特征,临床多诊断为前列腺增生症;该肿瘤预后差,多在诊断后数月死亡。目前文献较为公认的原发性前列腺淋巴瘤诊断标准为 :(1)淋巴瘤局限于前列腺及其周围软组织;(2)缺乏淋巴结累及表现;(3)在发现前列腺淋巴瘤之前,至少1个月之内未发现系统性淋巴瘤。
3.2病理诊断及鉴别诊断
IVLBCL的组织学特征是萎缩的前列腺腺体间质内,可见肿瘤样淋巴细胞位于血管内,多累及薄壁的毛细血管及小血管。肿瘤细胞生长模式可分为3种 :①肿瘤细胞位于血管腔内,远离血管壁生长,表现为失黏附性生长方式;②肿瘤细胞充满整个血管腔内,表现为黏附性生长方式;③肿瘤细胞沿着窦状隙播散方式。肿瘤细胞体积大,可见瘤巨细胞,细胞核深染,可见1~3个核仁,核分裂象易见。肿瘤细胞呈片状生长,少数可位于管腔外。免疫组化B细胞标记物CD20、CD79a和PAX-5阳性,血管内皮标记物CD31和CD34可显示肿瘤细胞位于血管腔内。
本例患者镜检示前列腺组织碎片内见扩张的毛细血管,血管内可见多量中-大淋巴样细胞,细胞异型性显著,细胞核呈卵圆形,染色质浓稠,可见少量胞浆,核分裂象可见,部分细胞退变、坏死;免疫组化结果示大细胞CD20和PAX-5均阳性表达,CD10阴性,Ki-67指数高表达,符合非霍奇金血管内弥漫大B细胞淋巴瘤,非生发中心来源;此外有关文献报道 ,相对于CD5阴性病例来说,CD5阳性者预后则较差,本例CD5阳性,皆提示病人预后很差。
前列腺IVLBCL与前列腺增生症伴炎症相鉴别 :(1)细胞学形态:炎症病灶的淋巴细胞体积小而深染,大小一致,细胞核膜光滑且完整、染色质细腻而均匀分布。本例患者初诊时因组织细胞挤压变形明显,忽略了异型淋巴样肿瘤细胞,从而误诊为前列腺慢性炎;(2)细胞密度和与周边腺体的关系:前列腺炎的淋巴细胞排列较为稀疏,可见较多的腺体,而淋巴细胞浸润于腺体之间;而淋巴瘤肿瘤细胞破坏了正常的前列腺结构,从而导致腺体数目减少;(3)免疫组化标记物:淋巴瘤为单克隆性增生,而前列腺慢性炎则为多克隆性增生;(4)前列腺炎患者在炎症活动期血清学PSA水平可升高,抗炎治疗后血清 PSA水平恢复正常,而前列腺淋巴瘤患者血清 PSA水平常在正常范围之内,该患者则如此。
IVLBCL需与DLBCL非特指型相鉴别 ,后者多表现为无痛性肿块,肿瘤细胞无独特的血管内生长方式,也需与以下肿瘤进行鉴别:(1)脉管内癌栓:常有临床原发病史,癌栓的表面有完整血管内皮被覆,或黏附于血管壁,肿瘤细胞常表达CK等上皮标记物。(2)血管内NK/T细胞淋巴瘤 :血管内淋巴瘤中85-90%为B细胞淋巴瘤,NK/T细胞淋巴瘤少见,免疫学标记物和TCR基因分子重排检测结果有助于二者的鉴别。(3)血管源性肿瘤 :增生的血管呈分叶状生长或吻合成迷路样,小血管腔内衬覆复层CD31/CD34阳性的内皮细胞,无异型淋巴样细胞黏附聚集于血管腔内。
3.3病因与发病机制
IVLBCL目前发病机制仍然不是很清楚,学术界主要存在着两种假说 :一种假说是肿瘤细胞由于缺少归巢因子和粘连分子,譬如CD29(整联蛋白因子)、CD54(细胞内黏附β因子)和CD11a等细胞因子;另一种假说是异型的淋巴细胞内缺少G蛋白耦合因子(CXCR3),还有小血管的内皮细胞内缺少趋化因子配体(CXCL9),目前这两种假说就解释了一些血管内B细胞淋巴瘤未能形成实体性肿瘤的现象,同时也能解释该肿瘤的高侵袭性生物学行为。但至于是何种原因导致了IVLBCL的肿瘤细胞易在小血管中积聚,目前还有待进一步探讨其发病机理。
IVLBCL 起源于转化的外周 B 淋巴细胞,免疫球蛋白基因呈单克隆性重排,部分病例分子学检测到细胞遗传学的异常,包括有 t( 11; 22) ( q23; q11. 2)、t( 3;14) ( q27; q32) 、t ( 14; 19) ( q32; q13) 等染色体基因易位,但目前研究还尚未发现有特征的遗传基因学改变 。
3.4治疗及预后
NCCN指南上弥漫大B细胞淋巴瘤一线治疗方案为 :①利妥昔单抗加CHOP(环磷酰胺、阿霉素、长春新碱、泼尼松);②剂量密度R-CHOP;③利妥昔单抗加EPOCH(足叶乙甙、泼尼松、长春新碱、环磷酰胺、阿霉素)等。目前临床研究资料显示R-CHOP方案明显提高了CD20强阳性的淋巴瘤患者的治疗效果,比传统CHOP方案治愈率提高了近20%。目前相关文献多采用该治疗方案,并且部分患者得到明显疗效。
总之,前列腺IVLBCL极其罕见,临床表现无特异性,多诊断为良性前列腺增生,从而导致漏诊。该肿瘤预后极差,多在确诊后数月死亡。病理形态学和免疫组化为该肿瘤的诊断金标准,早发现和早诊断能提高患者的预后。
参考文献略。
我要评论





共0条评论