我的博文
CAR-T细胞治疗被FDA踩刹车?
来源:医脉通
2016年6月7日,美国FDA紧急叫停一项关于抗CD19嵌合抗原蛋白T细胞(CAR-T)免疫治疗(JCAR015)急性B淋巴细胞白血病的中期临床试验。
CAR-T与CIK、DC-CIK、NK等非特异性细胞免疫治疗不同,它是一种特异性的细胞免疫疗法。从患者体内获得T淋巴细胞,通过技术手段将肿瘤抗原的高亲和性与T细胞的杀伤作用相结合,使T细胞获得特异性杀伤肿瘤细胞的能力,经过大量扩增后回输到体内。这种方式不需要MHC分子限制性地识别肿瘤潜在的抗原决定簇。
CD19特异性表达于恶性和正常B细胞以及B细胞前体细胞,而造血干细胞及非造血细胞则不存在CD19表达。因此针对CD19的CARs是目前临床上研究最多的CAR-T细胞。
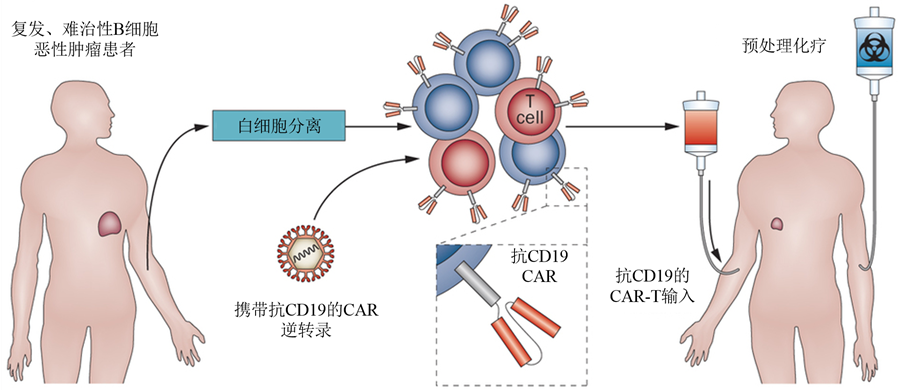
CAR-T细胞治疗在血液肿瘤中独领风骚,有研究显示应用针对CD19的CAR-T细胞治疗复发、难治性B细胞白血病,完全缓解率达到93% ( 55 /59 )。
而这项名为ROCKET的临床试验在将氟达拉滨加入预处理化疗方案后,2名患者死亡,因此被FDA叫停。当ROCKET研究开始时,预处理化疗方案仅有环磷酰胺一种药物。
为什么中途增加药物,开发JCAR015疗法的生物技术公司(JCAR015、JCAR014、JCAR017代表不同的CAR-T疗法)是这么解释的:由于多个研究均显示氟达拉滨联合环磷酰胺有疗效的改善,特别有JCAR014Ⅰ/Ⅱ期研究(晚期B细胞恶性肿瘤)和JCAR017Ⅰ/Ⅱ期研究(儿童ALL)的佐证,因而在后续试验中增加氟达拉滨。但是,自从添加了氟达拉滨,严重的神经毒性事件发生率增加,其中不幸地包括2名治疗相关脑水肿死亡的患者。
在2死出现后,FDA和数据安全监测委员会(DSMB)启动审查。而在这之前,2016年5月份已经出现了一例脑水肿死亡案例。评估了多个可能增加神经系统毒性的因素后,涉事公司认为主要原因还是在与氟达拉滨与JCAR015治疗联合。而预处理化疗仅含环磷酰胺时一直没有出现治疗相关死亡事件。
美国FDA要求涉事生物企业提交四份文件:修改的患者知情同意书、修改的研究者手册、修改的试验协议,以对针对此事向FDA做出的书面陈述副本。
值得注意的是,CAR-T虽然成为血液肿瘤领域免疫疗法的热门候选,但还要注意相关的配伍和毒副作用。本次叫停事件中,CAR-T疗法本身或许没有严重的缺陷,罪魁祸首可能是中途增加的化疗氟达拉滨。但是,特异性细胞免疫治疗的巨大前景和商业利益促使众多公司疯狂上马、大干快干,暴露出许多弊端令人深思。
我要评论





共0条评论