我的博文
ROS1阳性NSCLC靶向治疗进展 
1987年,ROS1基因在胶质母细胞瘤肿瘤的细胞株中被发现,ROS1是一种跨膜受体蛋白酪氨酸激酶,具有调节细胞凋亡、生存、分化、增殖、迁移和转化的功能1。
在NSCLC中迄今已发现至少有11种不同的ROS1融合基因,见图1,最常见的融合伴侣是CD741。ROS1融合基因与其它受体酪氨酸激酶具有共同的信号通路,见图2。
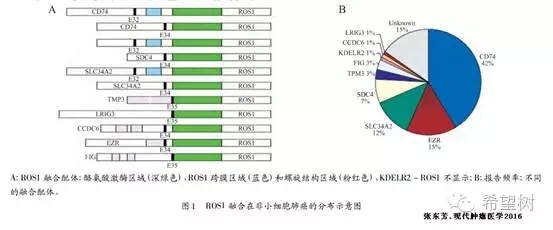
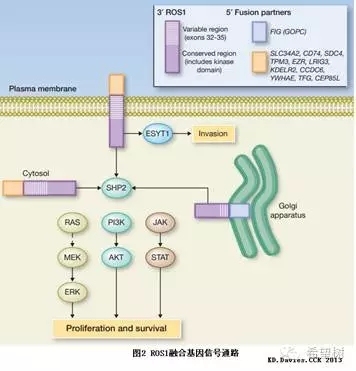
ROS1基因融合的临床病理特征
ROS1基因融合阳性在中国NSCLC中发生率约3.2%,与国外数据相近,多见于年轻、不吸烟的肺腺癌患者3,4。
ROS1基因融合阳性与ALK基因融合阳性或EGFR突变一般不会共存,也有文献报道ROS1 融合基因可以与其他基因突变共存,如EGFR突变5。
ROS1基因融合的检测
目前常用的ROS1基因融合阳性检测方法分为以下三种:荧光原位杂交(FISH)、RT-PCR和二代测序(NGS)。FISH法是金标准,但无法区分ROS1融合亚型,RT-PCR可检测多个融合伴侣,NGS可以检测任何融合伴侣6。免疫组织化学(IHC)无法区分ROS1野生和重排7。
ROS1基因融合的靶向治疗
ROS1基因和ALK基因在酪氨酸激酶区域序列存在49%同源性,而在激酶催化区的ATP结合位点二者同源性高达77%,因此有些ALK抑制剂同样具有ROS1激酶抑制活性7,见表1,28,9。
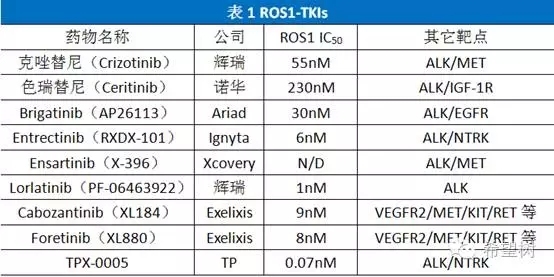
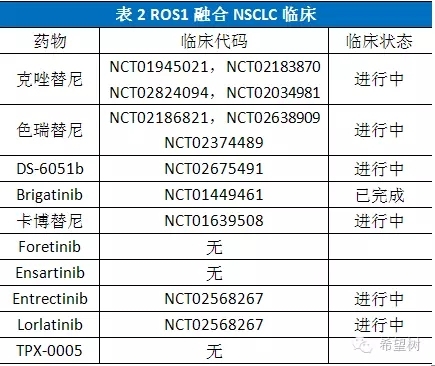
克唑替尼
PROFILE 1001一期临床数据显示,50例ROS1阳性肺癌患者,每天服用克唑替尼250mg Bid,3例完全缓解,33例部分缓解,客观缓解率为72%,中位无进展生存期19.2个月。在所检测的30例肿瘤标本中,研究人员发现了7个ROS1的融合伴侣,不同的ROS1融合类型与克唑替尼临床应答之间未观察到相关性10。2016年3月,美国FDA批准克唑替尼用于ROS1阳性的转移性NSCLC的治疗。
OO-1201是一项针对东亚人群的Ⅱ期临床研究,共入组127名ROS1阳性NSCLC患者,每天服用克唑替尼250mg Bid,客观缓解率88%,中位无进展生存期13.4个月,一年生存率84.4%,见图311。
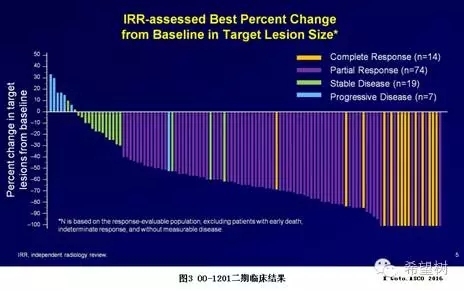
Lorlatinib
第三代ALK/ROS1抑制剂Lorlatinib能够克服ALK/ROS1耐药突变,而且具有强大的突破血脑屏障能力,目前已在进行治疗ALK阳性和ROS1阳性NSCLC患者的Ⅱ期试验12。
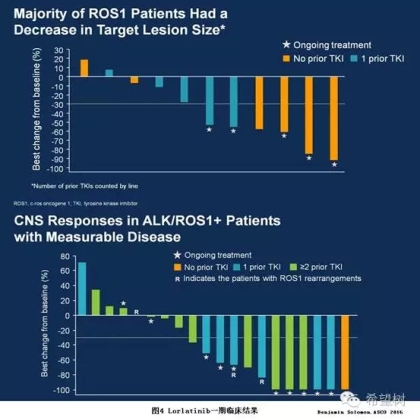
Entrectinib
Entrectinib是NTRK/ALK/ROS1抑制剂,具有强大的突破血脑屏障能力,目前已在进行治疗NTRK/ALK/ROS1阳性NSCLC患者的Ⅱ期试验13
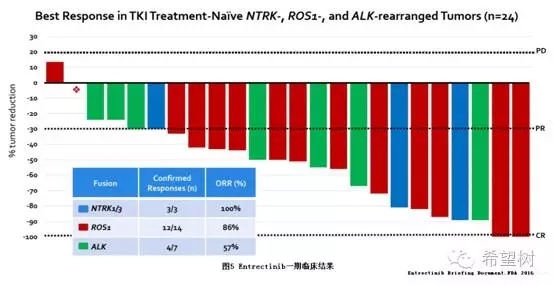
ROS1阳性NSCLC耐药机制
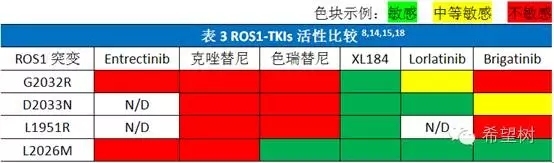
克唑替尼治疗ROS1阳性NSCLC的耐药机制主要是ROS1酪氨酸激酶结构域外显子36-42上的突变G2032R,D2033N,L1951R和L2026M等14,15,16,以及EGFR、KIT等信号通路激活17,18。
L2026M是守门员突变,D2033N 、G2032R和L1951R位于溶剂前沿,由于空间位阻效应和静电排斥作用的影响,削弱克唑替尼与ROS1基因之间的结合,导致耐药19。ROS1-TKIs抑制ROS1耐药突变的活性比较见表3。
美国麻省总医院的Gainor等用二代测序检测了10例克唑替尼耐药的ROS1阳性NSCLC患者的活检标本。10例患者中9例肺腺癌,1名肺鳞癌,中位无进展生存期为10个月。4例G2032R,1例D2033N,共占50%20。
卡博替尼
根据分子对接模式的不同,ATP竞争性酪氨酸激酶抑制剂可分为TYPE I型和TYPE II型。TYPE I型抑制剂模拟ATP的腺嘌呤环,通过与激酶“铰链”区域ATP结合位点形成1~3个氢键来识别激酶的活化构象,大部分ROS1抑制剂均是TYPE I型抑制剂,如克唑替尼、色瑞替尼等。TYPEII型抑制剂不但可以像TYPE I型抑制剂那样伸展到ATP 活性位点和“铰链”区域形成氢键,还可以同非活性构象形成的疏水口袋相互作用。小分子多靶点酪氨酸激酶抑制剂多数是TYPE II型抑制剂,如卡博替尼等21,22。
克唑替尼耐药实例1
1名CD74-ROS1阳性晚期肺腺癌,50岁女性,培美曲塞/顺铂/贝伐单抗三个疗程之后,服用克唑替尼,病灶缩小64%,18个月后脑转移,肺部病灶稳定,全脑放疗之后继续服用克唑替尼,8个月之后双肺结节影,纵隔及腹膜后淋巴结肿大。对腹膜后淋巴结进行活检取样,经二代测序(NGS)检测发现ROS1 D2033N突变,丰度14%,CD74-ROS1丰度70%,外周血阴性。患者参加了NCT01639508二期临床组,开始服用卡博替尼60mg每天,四周后复查,病灶部分缓解,12周后CT显示肺部病灶缩小92%。该患者服用卡博替尼一共8个月15。
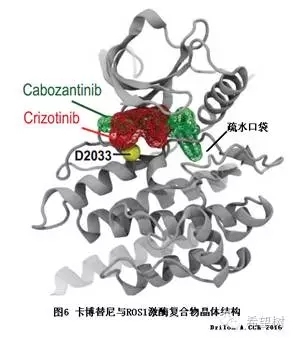
ROS1激酶结构域的某些位点常发生耐药突变,这些突变会导致肿瘤细胞对TYPE I型ROS1抑制剂如克唑替尼产生耐药。卡博替尼不仅占据ATP结合位点,还能通过守门员突变进入非活性“DFG-out”构象形成的疏水口袋,对产生耐药突变的ROS1基因仍具有抑制作用15,见图6。
NCT01639508临床组的标准剂量是60mg每天。卡博替尼40mg每天的剂量时,血药浓度高达643nM,足以抑制ROS1耐药突变21。
克唑替尼耐药实例2
1名ROS1阳性晚期肺腺癌,53岁女性,2011年11月确诊,左肺弥漫性病灶,纵隔淋巴结肿大,腹腔淋巴结转移,单发肝转移。她接受了6个疗程的培美曲塞联合顺铂化疗,接着6个疗程的培美曲塞维持治疗,肿瘤部分缓解。2012年10月进展后接受了6个疗程的吉西他滨联合卡铂化疗,接着特罗凯维持治疗。2013年9月进展后,左肺下叶穿刺进行基因检测,结果为ROS1融合阳性,开始克唑替尼治疗。2014年10月出现大量胸水,新增多发结节。胸水的基因检测结果显示,ROS1结构域没有突变,EZR-ROS1合并RNPC3-ROS1融合阳性。2014年12月开始服用卡博替尼,140mg每天,咳嗽和呼吸困难迅速缓解,二周后减量到120mg每天,再减量到80mg每天,一周后因为严重的手足综合症停药。停药一周后,因呼吸困难进行CT检测,发现双侧肺栓塞,4.3cm的原发病灶消失,右下叶病灶由1.7cm缩小到1.4cm。处置肺栓塞和手足综合症后,重新服用卡博替尼20mg每天。2周后CT复查显示病灶稳定,双侧胸腔积液少量增加。卡博替尼增量到40mg每天,60mg每天,后因肺栓塞复发而停药8。
转自:https://mp.weixin.qq.com/s?__biz=MzIzODA5NDUzNw==&mid=2648633224&idx=1&sn=3570bf3cc6afa0579a54bfa2b4d338d9&chksm=f114de2ec663573858254647e1c8544260da7c6bfdf909a3c29151dabda410a92d2d0c95b0ab&mpshare=1&scene=1&srcid=0219O7XBln1Y5r39MMJtBXxb&pass_ticket=GKHRxfyGEFNT%2Fu7b1yz3r9oYZRtGDdTj08I%2BgBgqHajqtIleD%2BDqxAiSd4cEaIcn#rd
我要评论





共0条评论